Qu’est-ce qu’une DCI ?
Tout médicament est caractérisé par :
- un nom
- une forme pharmaceutique (gélule, comprimé, sirop, etc.)
- un dosage
DCI, Dénomination Commune Internationale, correspond au nom de la substance active contenue dans un médicament. Elle est définie par l’OMS (Organisation Mondiale de la Santé) et permet d’éviter tout risque de confusion. Elle sert de langage commun à l’ensemble des professionnels de santé et des patients, quel que soit leur pays.
Prescrire en DCI, ce n’est pas prescrire un générique.
LA DCI = LE VRAI NOM SCIENTIFIQUE DU MÉDICAMENT !
Qu’est-ce qu’un médicament générique ?
Un médicament générique est un médicament qui comporte la (les) même(s) substance(s) active(s) au même dosage que le médicament deréférence, dit princeps.
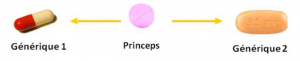
Les seules différences possibles entre princeps et génériques sont la forme pharmaceutique et les excipients.
Un excipient est une substance, autre que la substance active, qui consiste à donner un goût, une consistance ou une couleur au médicament. Il peut varier entre générique et princeps ou entre génériques.
PRINCEPS ET GÉNÉRIQUE = LA MÊME SUBSTANCE ACTIVE
= LA MÊME DCI
Repérer la DCI
Princeps (médicament de référence) :
NOM DE MARQUE
Générique :
Le générique peut se qualifier de 2 manières :
DCI + NOM DU LABORATOIRE
OU
NOM DE FANTAISIE + Gé ___
DCI
BIEN IDENTIFIER LA DCI, C’EST ÉVITER DE SE TROMPER EN NE PRENANT
PAS DEUX FOIS LA MÊME SUBSTANCE VIA 2 SPÉCIALITÉS DIFFÉRENTES
Qu’est-ce qu’un médicament biosimilaire ?
Un BIOSIMILAIRE est un médicament biologique développé pour être similaire à un médicament biologique de référence dont le brevet est tombé dans le domaine public.
On appelle médicament biologique ou biomédicament un médicament produit à partir d’organismes vivants.
Ils sont commercialisés à un prix plus bas que celui des médicaments de référence et sont utilisés depuis longtemps (2006) : on retrouve par exemple, l’insuline pour les patients diabétiques et plus récemment, des médicaments pour le traitement du cancer.
OUI ! Les BIOSIMILAIRES, c’est du sérieux !
-
- Des étapes de recherche et de fabrication qui durent près de 10 ans
- Des études de comparaison par rapport au biomédicament de référence qui sont analysées par les autorités de santé compétentes.
Pour être commercialisé, le BIOSIMILAIRE est évalué de manière très stricte par l’Agence Européenne du Médicament (EMA). Leur efficacité et leur sécurité sont donc démontrées et sont similaires à leur médicament de référence.
Source : ARS Centre, OMéDIT Centre, le CISS région centre, France Assos Santé centre Val de Loire.


 C.M.P.R.E. Bois-Larris
C.M.P.R.E. Bois-Larris